CuMn2O4 催化臭氧氧化實(shí)驗(yàn)材料與方法
近年來���,由于高級氧化技術(shù)可以產(chǎn)生大量活性氧組分 (ROS�����,如·OH、 SO4����、1O2 等)���,從而有效促進(jìn)痕量微污染物的降解,故而該技術(shù)成為降解高風(fēng)險微量有機(jī)物的重要手段�����,而且逐漸成為研究熱點(diǎn)����。雖然單一的臭氧氧化法能有效去除不飽和芳香族和脂肪族化合物,但其對飽和有機(jī)化合物的去除率很低�。為了高效去除難降解的飽和的持久性有機(jī)污染物,本文通過選用一種高性能的催化劑催化臭氧產(chǎn)生更多的活性物質(zhì)��,以達(dá)到徹底去除污染物的目的�����。
錳酸銅(CuMn2O4) 尖晶石是一種密度較大的空心六面體�,其晶體結(jié)構(gòu)主要是由Mn4+與Cu2+搭建的,還有較少的Mn3+與Cu+增加了結(jié)構(gòu)的缺陷程度�����。CuMn2O4 可以催化臭氧產(chǎn)生具有氧化能力強(qiáng)��、無選擇性的·OH,從而有效提高臭氧對水體中難降解污染物的去除效果���。有研究指出����,臭氧與CuMn2O4 的結(jié)合對二苯甲酮-3 的降解有明顯的協(xié)同作用��。然而��, 在實(shí)際使用過程中�����,CuMn2O4 的密度大�、容易團(tuán)聚、不易分散的特性使其利用率很低��。為了提高其利用率�,需要選用另外一種催化劑進(jìn)行耦合,彌補(bǔ)其在使用過程中的缺陷�����。研究表明��,二維層狀碳材料在催化臭氧氧化領(lǐng)域中有很好的效果�。因?yàn)槎S層狀碳材料不僅在平面內(nèi)的熱運(yùn)輸和電荷運(yùn)輸過程中具有突出的物理化學(xué)特性,而且與其他材料復(fù)合后可以產(chǎn)生良好的耦合效應(yīng)����。石墨烯/還原氧化石墨烯(rGO) 是其中一種極具吸引力的二維材料,具有卓越的化學(xué)穩(wěn)定性��、導(dǎo)電性和表面體積比���。
此外����,石墨相氮化碳(g-C3N4) 是一種具有2.7 eV 帶隙的二維非金屬聚合物半導(dǎo)體�����,在化學(xué)�����、熱和光照射過程中具有較好的穩(wěn)定性�����。同時,g-C3N4 還是一種有效的催化劑載體�,在其中摻雜選定的雜原子, 通過電荷轉(zhuǎn)移可以形成絡(luò)合的復(fù)合材料���。因此�����, 可以考慮將rGO 和g-C3N4 與CuMn2O4 進(jìn)行復(fù)合�����,應(yīng)用于催化臭氧氧化過程中���。與大多數(shù)親脂性的有機(jī)防曬劑不同的是,二苯甲酮-4(BP-4) 是一種親水性的紫外線吸收劑��,因其質(zhì)地更輕���、油性更少����,被廣泛應(yīng)用于洗發(fā)水、剃須凝膠��、止汗劑���、化妝品和牙膏等日用品中。但是��,由于BP-4 化學(xué)穩(wěn)定性好�、不易降解,因而被認(rèn)為是一種偽持久性有機(jī)污染物���,越來越受到人們的關(guān)注��。在目前的廢水處理領(lǐng)域中常見的水處理方法并不能將其完全去除�。此外��,由于rGO 和g-C3N4 在催化臭氧氧化過程中對臭氧氧化副產(chǎn)物溴酸鹽有很好的抑制效果��,因此�,本研究將rGO 和g-C3N4 與CuMn2O4 復(fù)合,來探究他們在催化臭氧氧化過程中對BP-4 的降解效果以及溴酸鹽生成的影響����。
1 材料與方法
1.1 實(shí)驗(yàn)原料及儀器
一水合硫酸錳(MnSO4·H2O,≥99.0%)、三水合硝酸銅(Cu(NO3)2·3H2O�����,≥99.0%)����、碳酸鈉(Na2CO3,≥99.8%)���、尿素(CO(NH2)2�����,99%)��、硝酸鈉(NaNO3�����,≥99.0%)�����、高錳酸鉀(KMnO4����,≥99.0%)、二苯甲酮-4(C14H12O6S��,98%)����、硫酸(H2SO4��,≥70%)�����、石墨粉����、過氧化氫(H2O2,≥27.5%) 和鹽酸(HCl�����,38%)����。
X 射線衍射儀;比表面積測試儀;X 射線光電子能譜儀�����;高效液相色譜儀���;智能箱式高溫爐�����;恒溫水浴振蕩器�;鼓風(fēng)干燥箱�����;電子天平��;pH 計����;離子色譜儀;電化學(xué)工作站����;磁力攪拌器�;電子掃描顯微鏡�����。
1.2 實(shí)驗(yàn)裝置
催化臭氧氧化BP-4 的效能實(shí)驗(yàn)采用間歇反應(yīng)模式進(jìn)行���。反應(yīng)器為圓柱形的玻璃容器���,直徑為6.2 cm,高為26.5 cm�����,有效容積為300 mL�。實(shí)驗(yàn)使用北京同林科技有限公司生產(chǎn)的
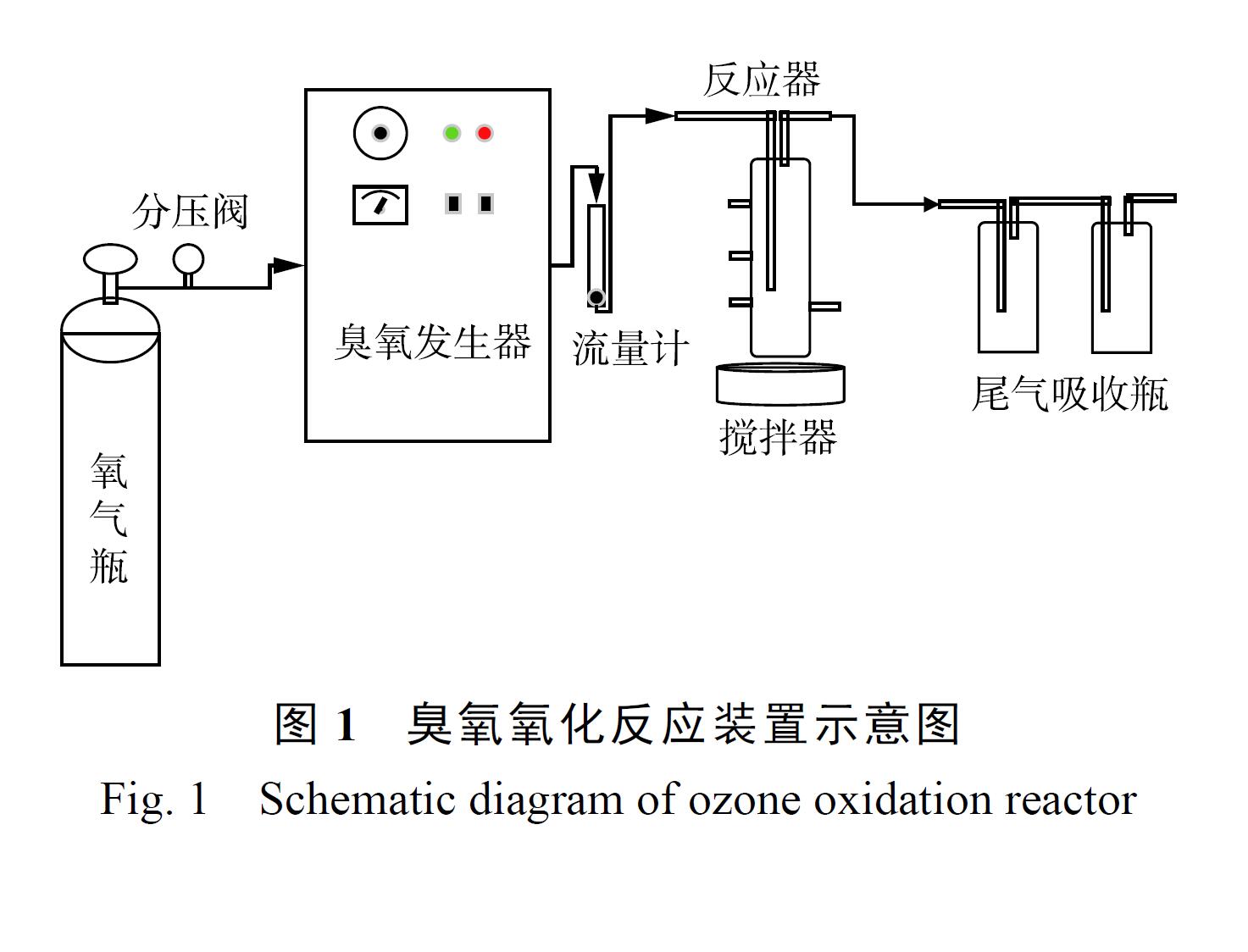
3S-A5 型臭氧發(fā)生器(臭氧產(chǎn)量為0~1 g·h−1)�,以高純氧氣為氣源,本實(shí)驗(yàn)所用的實(shí)驗(yàn)裝置如圖1 所示�����。實(shí)驗(yàn)中每次處理的水樣為300 mL�,所有的溶液均用去離子水配制。臭氧進(jìn)氣濃度通過臭氧發(fā)生器的放電功率來調(diào)節(jié)���。在每次實(shí)驗(yàn)開始之前�,用純氧進(jìn)行吹掃,并預(yù)臭氧化處理�����。打開臭氧發(fā)生器�����, 調(diào)節(jié)氣流量為400mL·min−1�����,臭氧發(fā)生器電流為0.025 A�,預(yù)熱時間為60 min,預(yù)臭氧時間為30 min����。
1.3 實(shí)驗(yàn)方法
在反應(yīng)器中加入290 mL 超純水,O3 曝氣30 min�����,攪拌器的轉(zhuǎn)速為800 r·min−1��。加入10 mL BP-4母液(反應(yīng)器中的濃度是0.084 mmol·L−1(25.91 mg·L−1));100 μL Br−母液(母液濃度為300 mg·L−1��,反應(yīng)器中的濃度是100 μg·L−1)�,開始反應(yīng)并計時。在反應(yīng)時間為0�、1、2����、5、7�、10、15����、30 min 時分別取樣��,并使用濃度為10 mmol·L−1 的亞硫酸鈉溶液還原殘留臭氧�����;使用0.22 μm 的水系濾膜過濾粉體催化劑后待分析��。
1.4 分析方法
使用X-射線衍射儀(XRD) 對制得的粉體催化劑的礦物組成與結(jié)晶結(jié)構(gòu)進(jìn)行分析���;使用比表面積分析儀對制得的粉末催化劑的比表面積及表面孔結(jié)構(gòu)進(jìn)行表征����; 使用X 射線光電子能譜儀(XPS) 表征粉末狀催化劑中各元素的價態(tài);使用電化學(xué)工作站分析粉末催化劑的阻抗��。使用掃描電鏡(SEM) 對制得的粉末催化劑進(jìn)行表觀形貌的分析�。
2結(jié)論
2.1使用兩步煅燒法成功制備出了CuMn2O4/rGO 與CuMn2O4/g-C3N4。通過XRD 表征��、BET 比表面積分析����、XPS 分析以及電化學(xué)交流阻抗測試分析發(fā)現(xiàn),盡管CuMn2O4/g-C3N4 比CuMn2O4/rGO 電子轉(zhuǎn)移速率更快�、氧空位更多,但是CuMn2O4/rGO 比CuMn2O4/g-C3N4 的結(jié)晶度更高�����、比表面積更大���、導(dǎo)電性更好����。
2.2 通過催化臭氧氧化降解BP-4 的實(shí)驗(yàn)結(jié)果表明,rGO 和g-C3N4 的摻入均能有效提升CuMn2O4催化臭氧氧化降解BP-4 的速率�����。但是��,二者的摻入對于溴酸鹽生成的控制效果有顯著差異����。在摻入rGO 后,溴酸鹽的生成量能進(jìn)一步減少��;而g-C3N4 的摻入對溴酸鹽生成的控制效果沒有提升����。
2.3進(jìn)一步比較CuMn2O4/rGO 與CuMn2O4/g-C3N4 的結(jié)構(gòu)和性能發(fā)現(xiàn),rGO 和g-C3N4 摻入CuMn2O4后可以阻礙了CuMn2O4 的團(tuán)聚的同時��,還可以作為一個高導(dǎo)電性的框架���,促進(jìn)CuMn2O4 在催化臭氧氧化過程中電子的轉(zhuǎn)移,此外����,由于其具有高導(dǎo)電性和大表面積而提高了催化效率��。綜合考慮2種復(fù)合催化劑對BP-4 的降解效果與對溴酸鹽的控制效果�,CuMn2O4/rGO 更適用于催化臭氧氧化��。